METABOLISME DE L'OXYGENE ET PRODUCTION D'ESPECES D'OXYGENE REACTIVES (ROS) et RADICAUX LIBRES
استقلاب الأوكسيجين وإنتاج الأنواع التفاعلية للأوكسيجين


Air:
21% de O2 (dioxygène)
Une espèce réactive de l'oxygène (Reactive Oxygen Species: ROS) est un radical oxygéné (O2•-, OH•) ou une molécule pouvant produire des radicaux libres oxygénés (H2O2). A L'opposé, il existe des radicaux libres azotés
(RNS).

ROS. Nomenclature

L'O2 est une molécule biradicalaire formée de deux atomes présentant sur leur orbitale externe deux électrons non appariés. Il est donc susceptible de capter facilement 1 puis 2 électrons pour être partiellement réduit en O2•- puis en H2O2. Il est ainsi à l'origine de la formation d'espèces réactives oxygénées (Reactive Oxygen Species : ROS).
En chimie, des radicaux libres sont des entités chimiques possédant un ou plusieurs électrons non appariés (électrons célibataires) sur leurs couches externes. Ils sont notés par un point '.'. Ils sont obtenus par rupture de liaisons chimiques. Cela peut arriver dans des cas de hautes températures,
radiations ionisantes et ultraviolets. La présence d'un électron célibataire confère à ces molécules une grande instabilité (elles ne respectent pas la règle
de l'octet), ce qui signifie qu'elles ont la possibilité de réagir
avec de nombreux composés. Si l'instabilité est importante,
l'électron libre est rapidement transféré sur une
autre molécule. le caractère radicalaire de la molécule
ne disparaît pas et l'électron libre peut passer sur d'autres
molécules, entraînant des phénomènes d'oxydation
en chaîne. C'est typiquement ce qui se passe lors de la peroxydation
des lipides.
Formation de radicaux libres secondaires
Le bilan de l'oxydation par l'oxygène moléculaire d'un substrat organique RH est le suivant :
RH + O2 ----> ROOH. C'est une réaction radicalaire en
chaînes dans laquelle les atomes d'hydrogène les plus
labiles du substrat sont arrachés par des radicaux libres. On
peut schématiser le mécanisme de la réaction comme
suit :
Amorçage:
production de radicaux libres amorceurs A·
A· + RH ---> AH + R·
Propagation: réactions en général très
rapides car les radicaux libres sont très réactifs.
R· + O2 ---> ROO· et ROO· + RH ---> ROOH
+ R·
Terminaison: réactions entre deux radicaux qui conduisent
à la formation de produits stables.
R· + R· ---> , ROO· + R· ---> et ROO·
+ ROO· --->. Tous des produits non radicalaires
Les
additifs limitant l'oxydation peuvent intervenir à deux
niveaux, à savoir dans la phase d'amorçage ou dans
la propagation des chaînes. Ils peuvent aussi simplement consommer
l'oxygène dans le milieu limitant l'oxydation : on
les appelle alors parfois antioxygènes.
En biologie, le terme de radical libre est utilisé pour désigner
les dérivés réactifs de l'oxygène, ou 'espèce
réactive oxygénée' (Reactive oxygen species
: ROS), ou 'radicaux oxygénés libres' ou 'dérivés
réactifs de l'oxygène'. Il s'agit d'une classe spécifique
de radicaux. Les exemples sont: le radical superoxyde O2. -, le radical
hydroxyle HO., les radicaux peroxyde (ROO.), le radical alkoxyle (RO.)
où R est une chaîne carbonée.
Les anions superoxyde (oxygène moléculaire ionisé
par addition d'un électron supplémentaire) sont des radicaux
libres de durée de vie très brève, sont très
toxiques pour les molécules biologiques, en particulier les acides
gras polyinsaturés, sur lesquels ils produisent des peroxydations
en chaîne.
Comment sont produits les ROS?

Ces espèces chimiques d'oxygène sont très instables et très réactives.
L'anion superoxyde (O2•-) est un radical chargé négativement provenant de la réduction monovalente de
l'oxygène moléculaire (O2) qui capte un électron.
La dismutation de cet O2•- entraîne la formation d'oxygène
fondamental et de peroxyde d'hydrogène (H2O2).
L'H2O2 n'est pas un radical libre au sens propre mais il est extrêmement réactif et possède un fort pouvoir oxydant. De plus, sa capacité à traverser les membranes biologiques fait qu'il peut se retrouver à une grande distance de son lieu de production.
Selon la réaction de Fenton, l'H2O2 se
décompose, en présence d'ions ferreux (Fe2+), en un ion OH- et un radical hydroxyle (OH.) [H2O2 + Fe2+ --> OH. + OH- + Fe3+]. Cette reaction s'interrompt rapidement par épuisement du fer ferreux, excepté en présence d'anion superoxyde (O2.-) qui régénère Fe3+ en Fe2+ selon la réaction d'Haber-Weiss [O2.- + Fe3+ --> O2 + Fe2+]. Ainsi, la présence simultanée de peroxyde d'hydrogene (H2O2), d'anion superoxyde (O2.-) et de fer
permet la production de radical hydroxyle (OH.).
L'OH•, avec une demi-vie de l'ordre de la nanoseconde,
est la plus instable et la plus réactive de toutes les espèces dérivées de l'oxygène. La diffusion limitée de ce radical lui permet de réagir avec de nombreuses espèces
moléculaires se trouvant à proximité (protéines,
lipides, ADN…) entraînant ainsi de multiples dommages cellulaires.
L'OH• apparaît comme l'espèce radicalaire ayant
un rôle majeur dans la cytotoxicité des ROS.
PRODUCTION DES ROS A L'ECHELLE DE LA RESPIRATION
En condition physiologique, la production de ROS reste faible et ne concerne qu'un faible pourcentage de l'oxygène capté par la respiration.

Les ROS sont principalement générés au niveau de la chaîne respiratoire mitochondriale. Parmi les différents paramètres modulant leur production, la nature des équivalents réduits (NADH,H+ et FADH2) et l'apport en oxygène sont essentiels.



Dans l'organisme, il existe de nombreuses sources de ROS parmi lesquelles:
- Autooxydation des petites molécules (dopamine, adrénaline, flavines et
hydroquinones). Le produit direct de ces auto-oxydations est souvent l'O2•-.
- Xanthine oxydase: Xanthine + 2O2 + H2O ---> Acide urique + 2 O2•- + 2H+.
- NADPH oxydase: 2O2 + NADPH ---> 2 O2•- + NADP+ + H+ (ex. phagocytes).
- Réticulum endoplasmique lisse: Le réticulum endoplasmique
lisse contient des enzymes qui catalysent une série de réactions
pour détoxifier les molécules liposolubles et d'autres
produits métaboliques toxiques. La plus connue de ces enzymes
est le cytochrome P450 qui oxyde les acides
gras insaturés et les xénobiotiques, produisant ainsi des ROS.
- Peroxysomes: Les peroxysomes sont une importante source de production d'H2O2 cellulaire. Toutefois, l'H2O2 est utilisé comme substrat de la catalase peroxysomale (enzyme antioxydante) afin de réaliser des réactions de peroxydation d'autres substrats. Ces réactions sont importantes dans le processus de détoxification présent dans le foie et le rein. Seule une faible quantité d'H2O2 produit au niveau du peroxysome pourrait échapper à la catalase.
PRINCIPAUX ORGANITES CELLULAIRES DE PRODUCTION DES RADICAUX LIBRES
| Dans Foie | Dans autres organes | |
| Mitochondrie | 15% | 45% |
| Peroxysome | 35% | 30% |
| Microsome | 45% | 20% |
| Cytosol | 5% | 5% |
D'où vient le superoxyde ?. L'excès de NADH ou d'O2 au niveau des mitochondries peut induire la réduction partielle de l'oxygène en ion superoxyde
Comment mettre fin au processus radicalaire ?. Les radicaux libres peuvent réagir entre eux pour mettre fin au processus radicalaire. C'est notamment le cas entre deux superoxydes (O2-) ou entre le superoxyde (O2-) et le monoxyde d'azote (NO):
--> La réaction superoxyde-superoxyde (dismutation) engendre du peroxyde d'hydrogène (H2O2). En effet, O2- est très oxydant; il peut dismuter en H2O2: 2 O2- + 2 H+ --> H2O2 + O2.
--> La réaction superoxyde-monoxyde d'azote produit du peroxynitrite (ONOO ).
D'autre part, les radicaux libres, étant instables, agiront en prélevant des électrons ou atomes d'autres molécules pour s'associer. Ainsi, ils peuvent attaquer le DNA
(ADN), les enzymes,
les protéines,
les membranes
cellulaires, .... Ces attaques peuvent être responsables
des états suivants:
* disfonctionnement lors de la réplication de l'ADN (DNA) entraînant
des mutations et cancers.
* perturbations au sein des cellules pouvant conduire à leur
mort.
* destruction des membranes cellulaires. Ceci peut entrainer le durcissement
et l'épaississement des artères conduisant aux crises
cardiaques.
* détérioration du collagène et rigidité
des tissus.
Ce n'est pas terminé! le Peroxyde d'hydrogène (H2O2) provenant de la dismutation du superoxyde peut former, en présence de sels de fer, le radical hydroxyle (OH.) qui est très
oxydant: Fe2+ + H2O2 ---> Fe3+ + OH. + OH- (réaction
de Fenton).
Radical hydroxyle (OH.), très oxydant,peux réagir avec des substrats organiques:
R + OH.----> ROH.
ROH. + Fe3+ .. ROH + Fe2+ (produits oxydés stables)
ROH. + ROH. ----> R-R + 2 H2O (produits 'cross-linked')
RH + OH. ----> R. + H2O
R. + O2 ---> ROO. (radical peroxyde)
ROO. + RH ---> R. + ROOH (réaction en chaîne)
ROOH + Fe2+ ---> RO. + OH- + Fe3+ (radical alcoxyle)
les réaction terminent avec des produits de cross-linking comme R-R ou ROOR.
Les ROS. AMIS ou ENNEMIS ?
Les radicaux libres peuvent être bons et mauvais. Ainsi, les radicaux libres dérivés de l'oxygène peuvent être bénéfiques pour l'hôte.
ROS = 'amis'
La production des ROS est indispensable à l'organisme en participant à divers processus vitaux tels que : la transduction de signaux cellulaires, la régulation des gènes et le fonctionnement de certaines enzymes, la défense immunitaire contre les agents pathogènes et la déstruction par apoptose de certaines cellules tumorales.

Voir --- > Maladie métabolique. Granulomatose chronique et NADPH oxydase.
ROS = 'énnemis'
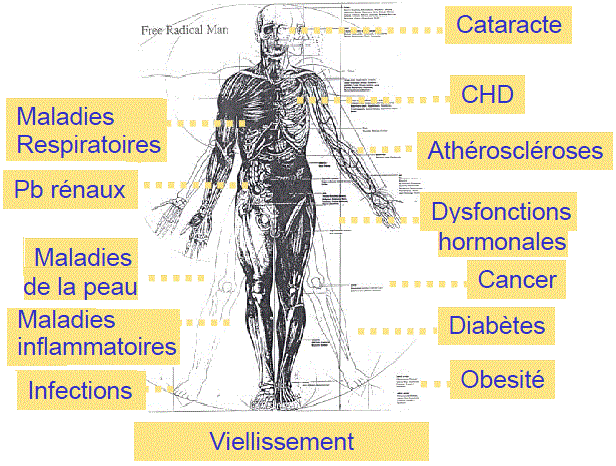


Parmi les différents paramètres pouvant moduler cette production de ROS, la nature et la proportion des équivalents réduits ainsi que la concentration en oxygène sont essentielles. Il est possible de modifier les apports en équivalents réduits par les régimes alimentaires et les apports en oxygène par l'hyperoxie.
LIENS UTILES
- Antioxydants et élimination des radicaux libres
مضادات الأكسدة و حذف الشقيات الحرة
- Antioxydants. Structure tridimensionnelle
بنيات مضادات الأكسدة
- Visualisation de la structure tridimensionnelle par JMOL
مضادات الأكسدة. بنية ثلاثية البعد
- Biotechnologies modernes. Applications
تطبيقات في البيوتكنولوجيات الحديثة
- Antioxydants de plantes. Articles (SMBBM congrès 2009)
- Stress oxydatif (oxydant) et antioxydants. Articles de congrès
- Biotechnologies modernes basées sur la technologie du DNA recombiné
- activites-antioxydantes.html

